Mapa Mental de Química sobre Atomística
Transcrição do Mapa Mental sobre Atomística
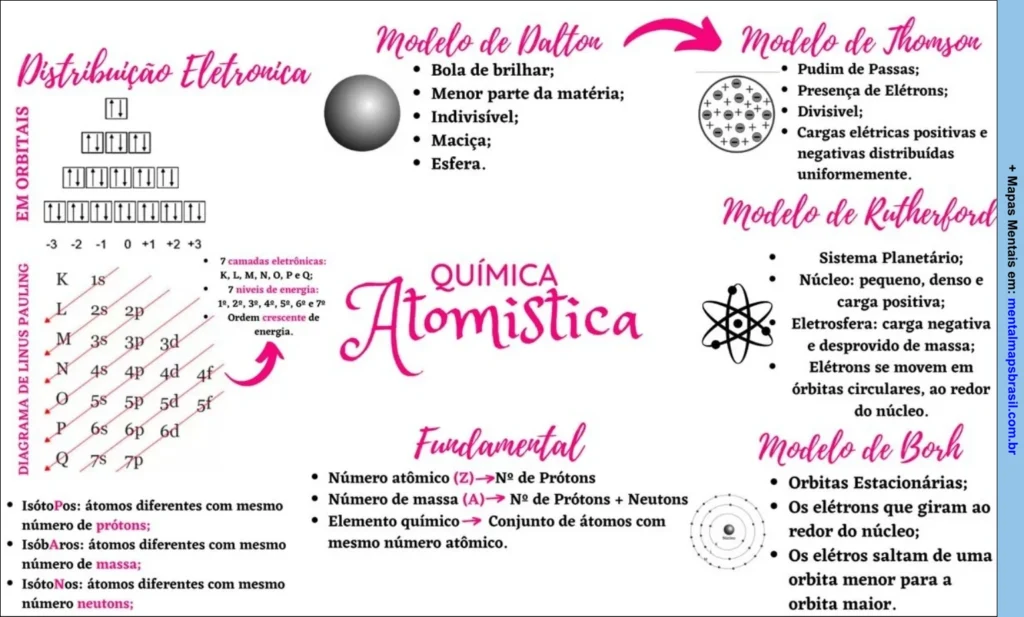
Distribuição Eletrônica EM ORBITAIS
[Diagrama visual de distribuição eletrônica em orbitais]
-3 -2 -1 0 +1 +2 +3
DIAGRAMA DE LINUS PAULING
K 1s
L 2s 2p
M 3s 3p 3d
N 4s 4p 4d 4f
O 5s 5p 5d 5f
P 6s 6p 6d
Q 7s 7p
Continue lendo…
7 camadas eletrônicas: K, L, M, N, O, P e Q;
• 7 níveis de energia: 1º, 2º, 3º, 4º, 5º, 6º e 7º;
• Ordem crescente de energia.
• IsótoPos: átomos diferentes com mesmo número de prótons;
• IsóbAros: átomos diferentes com mesmo número de massa;
• IsótoNos: átomos diferentes com mesmo número neutrons;
QUÍMICA Atomística
Modelo de Dalton
• Bola de brilhar;
• Menor parte da matéria;
• Indivisível;
• Maciça;
• Esfera.
Modelo de Thomson
• Pudim de Passas;
• Presença de Elétrons;
• Divisível;
• Cargas elétricas positivas e negativas distribuídas uniformemente.
Modelo de Rutherford
• Sistema Planetário;
• Núcleo: pequeno, denso e carga positiva;
• Eletrosfera: carga negativa e desprovido de massa;
• Elétrons se movem em órbitas circulares, ao redor do núcleo.
Fundamental
• Número atômico (Z)→ Nº de Prótons
• Número de massa (A)→ Nº de Prótons + Neutons
• Elemento químico → Conjunto de átomos com mesmo número atômico.
Modelo de Bohr
• Orbitas Estacionárias;
• Os elétrons que giram ao redor do núcleo;
• Os elétros saltam de uma orbita menor para a orbita maior.
Mapa Mental sobre Átomo e Propriedades com Explicação da Tabela Periódica

Transcrição do Mapa Mental sobre Atomistica – Estudo do átomo e suas propriedades
Conceito
Número Atômico – Z ou P
Número que indica a quantidade de prótons no núcleo atômico.
Número de Massa – A
Soma dos prótons e nêutrons no núcleo de um átomo.
A = Z + n
Representação dos Átomos
Átomo no Estado Fundamental
Átomo eletricamente neutro.
z = nº de elétron
Continue lendo…
Íons:
Cátion (+): Íon positivo – Perde elétron
Ânion (–): Íon negativo – Ganha elétron
Semelhanças Atômicas:
- Isótopos – P de próton
Átomos com o mesmo número de prótons.
Obs.: Prótons = Z - Isótonos – N de nêutron
Átomos com o mesmo número de nêutrons.
Obs.: Prótons ≠ Massa - Isóbaros – A que corresponde a massa
Átomos com o mesmo número de massa.
Obs.: Prótons ≠ Massa - Isoeletrônicos – E de elétron
Átomos com o mesmo número de elétrons.
Distribuição Eletrônica
Camadas ou Níveis:
Camada: K L M N O P Q
Nº máx. de e: 2 8 18 32 18 8 2
Subcamada ou Subnível:
Subnível: s p d f
Nº máx. de e: 2 6 10 14
Diagrama de Linus Pauling
Linus Pauling propôs um diagrama prático de distribuição eletrônica. Os e são distribuídos em ordem crescente de energia em níveis e subníveis na eletrosfera do átomo.
Tabela Periódica
- Elementos Representativos
- Elementos de Transição
- Transição Externa
- Série dos Lantanídeos
- Série dos Actinídeos
- Transição Interna
7 Linhas: Séries ou Períodos
- Mesmo número de camadas
18 Colunas: Famílias ou Grupos
- Propriedades semelhantes
- Mesma terminação na distribuição
- Metais Alcalinos
- Metais Alcalinos Terrosos
- Família do Boro
- Família do Carbono
- Família do Nitrogênio
- Família dos Calcogênios
- Família dos Halogênios
- Família dos Gases Nobres
Exemplos de Distribuição
Veja a distribuição de um átomo de Bário que possui 56 elétrons como exemplo:
K: 2 L: 8 M: 18 N: 18 O: 8 P: 2
Elétron de Valência
Só sai e entra na ÚLTIMA CAMADA:
S: 1s²
Fe²: 1s² 2s² 2p⁶ 3s² 3p⁶ 3d⁶ (cátion)
Fe³: 1s² 2s² 2p⁶ 3s² 3p⁶ 3d⁵ (cátion)
Cl: 1s² 2s² 2p⁶ 3s² 3p⁵ (ânion)